Ved Stanford University School of Medicine i California forskes det på en behandling som kan brukes mot flere typer av kreftsvulster. Forskerne rapporterte for et år siden at de kan ha utviklet en behandling som kan krympe eller kurere svulster i blære, bryst, eggstokk, hjerne, lever, prostata og tykktarm.
Anført av biologen Irving Weissman, MD, undersøkte en gruppe forskere kreftceller fra ulike svulsttyper. Nesten alle kreftcellene var beskyttet av et protein kalt CD47. Dette hadde Dr. Weissman studert tidligere i tilknytning til leukemi og lymfom (lymfekreft).
CD47 er en slags “ikke ødelegg meg”-markør som normalt finnes på friske blodlegemer. Denne markøren hindrer immunsystemet i å angripe blodlegemene der de sirkulerer rundt i kroppen med blodet eller ute i vevet. Weissman fant imidlertid at CD47 også var tilstede i høye nivåer på leukemi- og lymfom-celler, noe som gjør dem praktisk talt usynlig for makrofagene. Makrofager er en type immunceller som er programmert til å beskytte kroppen mot skadelige patogener (sykdomsfremkallende organismer), og som også fjerner kroppsceller som har blitt gamle eller skadet og dermed ikke fungerer som de skal. For eksempel, røde blodlegemer starter med mye CD47 på celleoverflaten når de er unge, men sakte mister de CD47 ettersom de blir gamle. På et tidspunkt er mengden av CD47 på overflaten av et aldrende rødt blodlegeme ikke nok til å demme opp for makrofagene. De eldre cellene blir fortært og ødelagt, noe som rydder vei for nye røde blodlegemer. -En del av kroppens renovasjonsvesen, rett og slett.
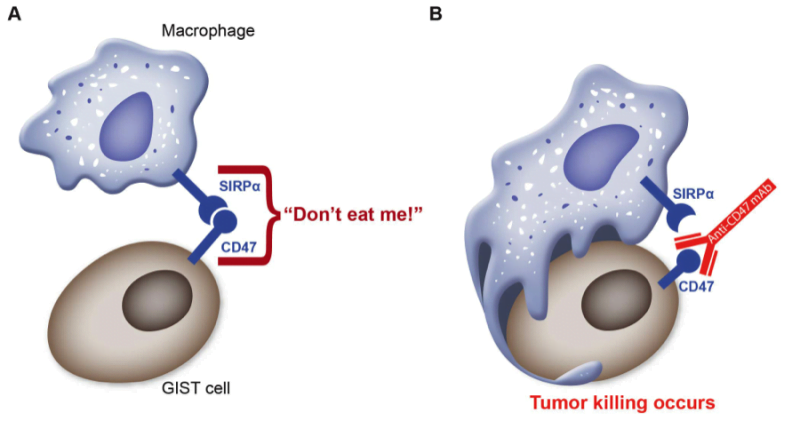
Ved å blokkere CD47 oppdaget Weissman at han kunne omskolere immunsystemet til å gjenkjenne kreftcellene som kreftceller og deretter angripe dem etter behov. Nysgjerrig på om dette samme prinsippet kunne brukes mot flere krefttyper tok Weissman og teamet hans kreftceller fra blære, bryst, eggstokk, hjerne, lever, prostata og tykktarm og dyrket dem i petriskåler, tilsatte noen av skålene først et antistoff mot CD47 og deretter makrofager (i alle skålene).

Testen var om antistoffet bandt seg til CD-47-molekylene og dermed blokkerte «ikke-spis-meg»-signalet til makrofagene. Og testen fungerte: Uten antistoff i skålene lot makrofagene kreftcellene være i fred; med antistoff tilstede angrep de og spiste cellene. “Det vi har vist er at CD47 ikke bare er viktig på leukemi- og lymfomceller,” fortalte Weissman. “CD47 er på hver eneste humane primære svulst som vi testet.” (Human betyr her «fra mennesker», ikke at svulsten er hensyntagende. Primær svulst betyr at de har testet celler fra hovedsvulsten, ikke fra metastaser. Primær betyr «den første» eller «hoved»-etellerannet.)
Forskerne implanterte (sprøytet inn) deretter humane tumorceller i mus, slik at kreftcellene fikk vokse litt før musene fikk CD47-antistoff. De fant at behandlingen hemmet utviklingen av nesten alle tumores som ble undersøkt, og hindret metastaser (spredning) til andre deler av kroppen. Blant mus med blærekreft, for eksempel, hadde bare en av 10 som fikk antistoff, lymfeknuter med tegn på kreft. I kontrollgruppen hadde 10 av 10 mus kreftceller i lymfeknutene.
I noen tilfeller – særlig tykktarm og brystkreft – hadde antistoffet til og med krympet eller eliminert svulstene helt. “Vi viste at selv etter at svulsten har tatt tak, kan antistoffet enten kurere svulsten eller bremse veksten og hindre metastasering, ” fortalte Weissman. Resultatene er absolutt lovende, men andre krefteksperter advarer mot å bli for begeistret for tidlig.
En ting er at det kan være uønskede bivirkninger til behandlingen. Som med cellegift, for eksempel, risikerer du ikke bare å drepe svulsten, men også de normale cellene. Weissman og teamet hans erkjenner at dette er en mulighet, men rapporterer at ødeleggelsen av normale celler synes å være et midlertidig problem. I deres studie var musene i stand til å skru opp produksjonen av nye celler for å erstatte de tapte gjennom behandling.
«En større bekymring», sier forsker Tyler Jacks, PhD ved Massachusetts Institute of Technology, «er at behandlingen kan være mindre effektivt hos mennesker enn hos mus. Mikromiljøet til en ekte svulst er noe mer komplisert enn mikromiljøet til en transplantert svulst. Det er mulig at en reell svulst har ekstra immun-undertrykkende effekt.”
Dette vil Weissman snart finne ut. Han og hans team har fått 20 millioner dollar fra California Institute for Regenerative Medicine til å ta forskningen sin videre fra musestudier.” Vi har nok data allerede til at jeg kan si jeg er trygg på at dette vil gå til fase I-studier på mennesker”, sa Weissman. For nøyaktig en uke siden (31.03.14) kom det en oppdatering på dette forskningsprosjektet. Der sier Weissmann og hans forskergruppe: «Slik det ofte skjer under utviklingen av nye behandlingsformer, har ulike komplikasjoner forskjøvet den planlagte startdatoen for de kliniske studiene. Selv om vi hadde håpet å starte kliniske studier i første halvår i år, var vi klar over at uforutsette forsinkelser kunne bremse fremgangen, og vi håper nå virkelig at kliniske studier vil starte sommeren eller tidlig høst 2014.»
De første utprøvingene av nye behandlinger på mennesker betegnes «kliniske studier fase I». Dette er svært små studier på bare noen få pasienter, for å sjekke sikkerheten til behandlingen – om den er mer skadelig enn helsebringende. Forskerne ønsker å understreke at dette dessverre betyr at bare en liten brøkdel av de pasientene som er interessert vil bli inkludert i første fase I kliniske studier. Følgelig oppfordrer de pasienter til å fortsette å utforske eksisterende behandlinger og andre kliniske studier.
