Cellegift er noe herk. Enda mer herk blir det hvis den ikke virker likevel, tross alle plagene.
På den årlige europeiske urologi-kongressen som for tiden pågår i Milano presenterte W. Tan og kolleger sin studie på neoadjuvant (= forbehandling med) cisplatin-basert kjemoterapi. Studien viste at epigenetiske forandringer spiller en nøkkelrolle i utviklingen av kjemoresistens i blærekreft.
Jaha?
Kjemoresistens betyr at cellegiften ikke virker lenger, akkurat som antibiotikaresistente bakterier ikke lar seg knekke av antibiotikaen. Kreftcellene har rett og slett funnet en måte å beskytte seg på, og overlever behandlingen.
Men epi-genetiske forandringer? -Vi har hørt om genetikk, holder ikke det?
Her må vi nok inn med en litt lengre forklaring, heng med: Genene (DNA-et) er et system av lange kjeder av byggeklosser som kan settes sammen etter visse regler. De gir oss oppskriften på hvilke proteiner vi skal produsere i cellene våre. Utvalget av proteiner bestemmer hvilke elementer organismen vår består av, for eksempel at øyefargen din er blå mens min er grønn.
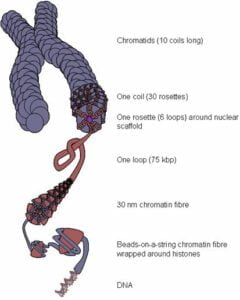 Men vi trenger noe mer. Vi trenger et styringssystem som slår disse genene av og på ettersom de trengs. For å holde orden på metervis med tynn (og da MENER jeg tynn!) tråd inne i hver cellekjerne, har naturen laget seg et fenomenalt pakkesystem for disse trådene. Først spoles de opp på noen små protein-trådsneller som tar noen få runder med tråd hver og sitter tett i tett bortover, akkurat som et perlekjede. Dette perlekjedet blir så tvunnet opp i en litt tykkere kveil, og så blir den kveilen tvunnet opp enda en gang, til en enda litt tykkere kabel. Ett fedd DNA-tråd, rett og slett (du har vel svart belte i strikking?).
Men vi trenger noe mer. Vi trenger et styringssystem som slår disse genene av og på ettersom de trengs. For å holde orden på metervis med tynn (og da MENER jeg tynn!) tråd inne i hver cellekjerne, har naturen laget seg et fenomenalt pakkesystem for disse trådene. Først spoles de opp på noen små protein-trådsneller som tar noen få runder med tråd hver og sitter tett i tett bortover, akkurat som et perlekjede. Dette perlekjedet blir så tvunnet opp i en litt tykkere kveil, og så blir den kveilen tvunnet opp enda en gang, til en enda litt tykkere kabel. Ett fedd DNA-tråd, rett og slett (du har vel svart belte i strikking?).
All tvinningen skjer ved hjelp av proteiner som støtter og bygger og hjelper. Ytterst blir det til slutt lagt på et beskyttende lag med proteiner og noe som kalles metylgrupper (og noen andre små kjemiske småttinger). Du kan kanskje se for deg en masse isoporkuler som har festet seg utenpå en tykk kabel?
Når genene skal leses av for å bli brukt, må metylgruppene fjernes. Det betyr at når disse metylgruppene sitter på DNA-tråden, viser de områder med avslåtte gener. Når vi finner et mønster av hypermetylerte (massevis av isoporkuler) eller hypometylerte (ingen isoporkuler) gener hos en gruppe pasienter og det motsatte hos en annen gruppe pasienter, for eksempel de som responderer og de som ikke responderer på en behandling, har vi et spor å gå etter når det gjelder å finne ut hvilke gener som styrer denne egenskapen. Slike områder er det Tan og kompani har funnet.
Tilbake til studien:
Ifølge forskerne vil det å finne en markør som er i stand til å forutsi respons på behandling, øke «den komplette patologiske responsraten». Det betyr at de som behandles har en bedre gjennomsnittlig respons fordi man behandler de rette personene og sparer ikke-respondenter for bivirkninger av cellegift som de ikke har nytte av. DNA-hypermetylering har tidligere vært koblet til kjemoterapiresistens i kreft.
“Vi satte opp en hypotese om at DNA-metylering ikke bare kan representere mekanismer for erverv av motstand, men også kan være en mulig biomarkør for å forutsi respons til platinum-basert kjemoterapi i blærekreft,” skrev forsker Tan. I studien ble DNA ekstrahert fra 48 muskelinvasive blæresvulster, tatt før pasienten mottok platinum-basert neo-adjuvant kjemoterapi. Alle svulster innholdt > 80% tumorceller.
Ifølge forskerne antyder analysen at ervervet resistens er assosiert med global hypermetylering i både primære tumorer og parede cellelinjer. En såkalt SVD (Singular value decomposition )-analyse viste at den sterkeste metyleringssignaturen var assosiert med kjemoterapirespons (p = <0,001).
Forskerne fant ~ 2700 «metyleringsvariable posisjoner» (MPVer, altså områder på DNA-trådene med bestemte egenskaper) som var assosiert med kjemoterapirespons. Hierarkisk clustering (gruppering) av disse MVPene definerte tre klynger, 1) kjemosensitiv, 2) kjemoresistent og 3) en blandet gruppe med hypometylerings-fenotype. MVPene assosiert med resistens omfatter nye gener som MEIS2, PROM1 og MAP1LC3A samt gener tidligere assosiert med resistens i andre svulster, som for eksempel MEST og MLH1.
“Disse data tyder på at epigenetiske forandringer er potensielt viktige drivere i utviklingen av cellegift-resistens i blærekreft. I tillegg til å gi ny innsikt i mekanismer for resistens, har vi identifisert mulige biomarkører for videre evaluering i fremtidige kliniske studier, inkludert potensielle stratifiseringsbiomarkører i kliniske studier av epigenetiske behandlingsformer som reverserer den ervervede resistens-fenotype, ” konkluderte forskerne.
Det betyr noe sånt som at de ser muligheter for å finne ut nøyaktig hvilke gener de skal se etter for å kunne bestemme hvem som kan ha nytte av cisplatin-basert cellegift, gjennom studier av medisiner som kan hindre – eller til og med reversere – utvikling av kjemoresistens.
Presseoppslaget ligger her, med referanse og alt.
